近日,芬兰骨科器械公司 Bioretec宣布,其基于镁合金平台技术的可生物降解植入物 RemeOs DrillPin获得美国FDA 授予的 “突破性设备认定”(Breakthrough Device Designation)。该产品适用于儿童及成人患者的骨折块固定,尤其覆盖 ≥2 岁、存在开放性生长板的儿童干骺端骨折,包括临床上长期被视为高风险场景的 跨生长板(经骺线)固定适应症。

这是 Bioretec 第三款获得 FDA 突破性设备认定的产品。在此之前,其 RemeOs 创伤螺钉与椎间融合器已分别于 2021 年和 2024 年获此认定,其中创伤螺钉已获得美国医保 CMS 的通行支持,具备明确的商业化基础。这一系列进展,标志着 Bioretec 的镁基可降解金属平台,正在从“材料创新”逐步进入 临床、监管与支付体系共同认可的阶段。
# 临床背景:跨生长板固定,为何长期缺乏理想解决方案
在儿童骨科领域,骨折治疗始终存在一个难以回避的核心矛盾:既需要足够稳定的内固定,又必须避免对生长板造成长期损伤。 传统金属植入物(如钢针、钛合金螺钉)在力学性能上能够满足固定需求,但一旦跨越生长板,可能带来生长障碍、骨骼不对称甚至畸形风险。因此,临床上往往需要在骨折愈合后进行 二次取出手术。而对儿童患者而言,这意味着额外一次麻醉、手术创伤和感染风险,也增加了家庭和医疗系统的负担。 可吸收高分子材料虽然在“无需取出”方面具备优势,但在负重能力、固定稳定性和适应复杂骨折方面仍存在明显局限。 正因如此,“既能提供金属级固定强度,又能在愈合后自然退出体内”的解决方案,长期被视为儿童骨科的理想目标,却始终缺乏成熟可用的产品。

# 产品与技术:RemeOs DrillPin 的工程逻辑
RemeOs DrillPin 所依托的,并非传统意义上的可吸收材料,而是一种 可生物降解的镁合金金属平台。这一技术路线的关键,在于同时解决“强度”和“退出机制”两大难题。 从力学层面看,RemeOs 镁合金在植入早期可提供接近传统金属的固定强度,能够满足骨折初期对稳定性的要求;随着骨愈合进程推进,材料逐步发生可控降解,其力学支撑能力与骨重建节律相匹配,避免“提前失稳”或“长期异物残留”。
从生物学层面看,镁在体内降解释放的离子被认为具有一定的 骨诱导促进作用,有助于骨形成与重塑。相比惰性金属植入物,这种“生物活性”使其更接近骨愈合过程中的自然参与者。 在临床使用层面,RemeOs DrillPin 具备良好的影像学兼容性,不影响 X 光或 CT 评估,并具备 MRI 条件安全属性,减少了术后随访中的限制。更重要的是,其 无需二次取出手术的特性,对儿童患者尤其关键,也正是其在跨生长板固定场景中被寄予厚望的原因。
# 公司视角:从单一产品到平台化路径
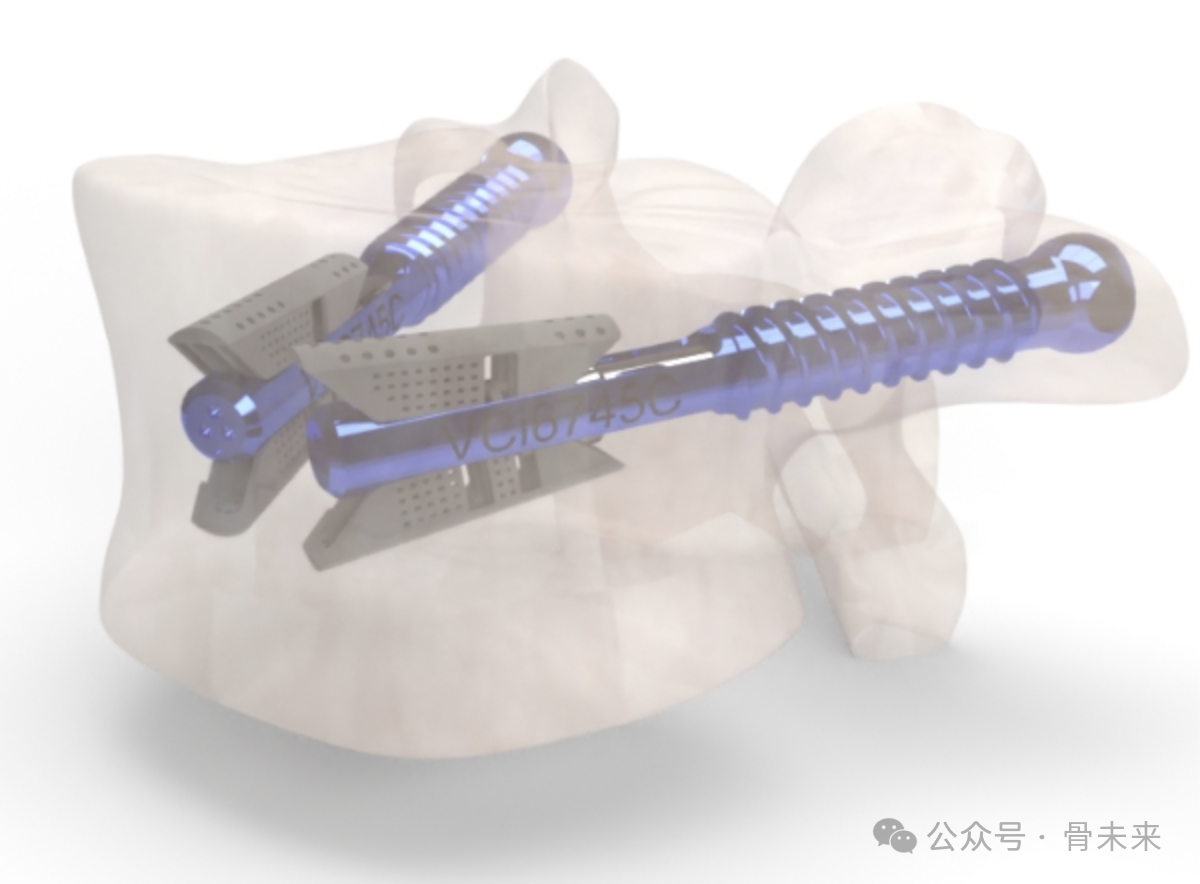
Bioretec 的长期定位,是通过 完全可生物降解植入物重塑骨科手术中“固定—愈合—退出”的完整生命周期。围绕这一目标,公司在活性植入物的生物界面工程方面形成了独特能力,将材料科学、力学性能与骨生物学过程进行系统协同。 从创伤螺钉,到 DrillPin,再到椎间融合器,RemeOs 系列产品已覆盖创伤骨科、儿童骨科及脊柱等多个高价值场景,也为镁基可降解金属在更广泛骨科应用中的可行性提供了持续验证。
# 观察:可降解金属,正在进入最保守的临床领域
从行业视角看,RemeOs DrillPin 获得突破性设备认定的意义,已超越单一产品本身。儿童骨科,尤其是涉及生长板的治疗,一直是 最谨慎、最保守的临床领域之一。一种新材料、新路径能够在这一领域获得监管层面的明确支持,本身就释放出强烈信号。 这意味着,可降解金属技术正在从“材料是否可行”的讨论阶段,进入“是否能被纳入标准治疗路径”的现实检验阶段。它不再只是对传统金属的替代,而是在重新定义骨折固定的终点形态——在完成使命后自然退出,而非永久留存。










