01、研究背景
高纯镁凭借可调控降解、优异生物相容性与良好促成骨能力,已成为可吸收引导骨再生屏障膜的理想候选。然而,将镁基屏障膜暴露于口腔环境中面临重大挑战,如口腔生理微环境会影响腐蚀速率、细菌附着以及生物膜的形成。这些因素可能会影响屏障膜的腐蚀降解过程及机械完整性,并阻碍组织再生。镁的降解与口腔微生物生态之间的双向相互作用目前仍不清楚。现有体外抗菌数据因缺乏唾液流变、宿主免疫及共生菌竞争等真实口腔参数,难以预测体内行为,导致镁基金属在口腔内的抗菌效能、降解腐蚀行为缺失统一标准。
对此,广州医科大学李平教授、Janak Lal Pathak教授与南方医科大学张文泰研究员、暨南大学于振涛教授等人通过原位验证模型,将早期生物膜群落与镁腐蚀产物释放过程关联,解析镁的降解与口腔微生物生态之间的双向相互作用。结果表明:镁-细菌相互作用会诱导形成以生物矿化沉积与有机基质整合为特征的空间异质腐蚀层;动态唾液流动与生物膜屏障协同促进均匀电化学降解,抑制局部点蚀。纯镁在口腔内因唾液螯合与成熟生物膜作用而抑菌效果减弱,并导致材料表面微生物定植呈现个体差异。本研究阐明了人体口腔微生物组在调控镁腐蚀路径中的关键作用,为镁基屏障膜的合理设计提供了重要参考。
02、图文导读
本文通过对比无菌BHI培养基(空白组)、细菌接种组(体外组)及人体口腔环境(原位组)中镁的腐蚀行为,系统阐明了不同环境对腐蚀过程的影响。扫描电镜及元素分析(图1)表明:无菌BHI培养基形成致密均匀的腐蚀层,O、C、P分布均匀;细菌接种组腐蚀层薄且不均,P仅局部沉积;口腔暴露组表面形貌最均匀,但O、P分布不均,呈现高O低P区域,说明细菌破坏腐蚀产物的稳定性。
XRD与XPS分析进一步揭示组成差异:三组腐蚀产物均以CaCO3和Ca10(PO4)3(CO3)3(OH)2为主(图1B),但Mg(OH)2仅出现在细菌接种组,原位组中未检出。XPS结果显示口腔组腐蚀层外层C、N含量显著偏高,而Mg、P信号极弱(图1C、D),表明其最外层以有机物为主。综上,无菌环境利于形成稳定无机腐蚀层;细菌介入破坏结构均匀性并促进Mg(OH)2生成;真实口腔环境中微生物群落导致腐蚀层外缘有机化,且无机元素分布紊乱,凸显微生物对镁腐蚀行为的复杂调控作用。
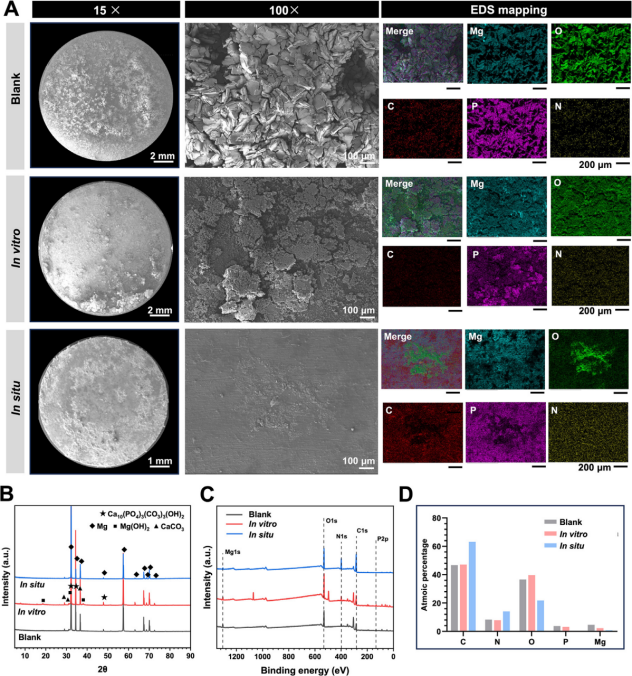
图1 对在不同条件下镁(Mg)金属表面的腐蚀形貌及产物分析
为评估镁金属在不同环境下的腐蚀行为,本研究进行了电化学分析。Bode相位图(图2A)显示:未处理样品在中频区呈单一尖锐峰,对应未处理镁金属表面;所有处理样品则呈现宽峰,反映腐蚀产物层引起的多重时间常数。等效电路拟合采用Rs(QctRct)(未处理)和Rs(Qp(Rp(QctRct)))(处理)模型,关键参数Rct值变化揭示:未处理组最低(1.3 kΩ·cm²),无菌BHI组升至2.5 kΩ·cm²,表明保护层形成;细菌接种组降至1.53 kΩ·cm²,证实微生物破坏作用;口腔原位最高(3.16 kΩ·cm²),提示致密生物矿化层生成。此趋势与Bode阻抗图低频区总阻抗一致(图2B)。Nyquist图(图2C)中,细菌接种组低频区出现感抗弧,暗示局部腐蚀;口腔原位组则呈扩散控制特征,反映致密保护层限制电解液渗透。极化曲线(图2D)进一步验证:无菌BHI组腐蚀电位正移至-1.81 V,电流密度降至1.85×10⁻⁵ A/cm²;细菌接种组参数接近未处理状态(-2.00 V,4.24×10⁻⁵ A/cm²);口腔原位组表现最优(-1.66 V,1.91×10⁻⁵ A/cm²),证实其高保护性生物矿化层可有效抑制电化学降解。
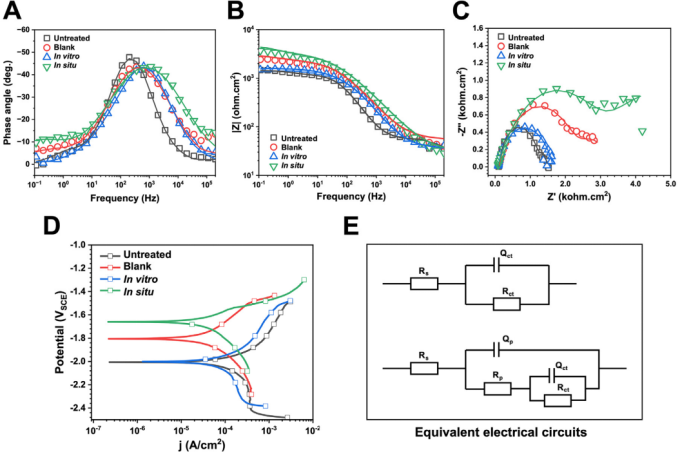
图2 在不同条件下对镁(Mg)金属进行的电化学测试
为全面评估镁金属的原位抗菌性能,本研究采用多样化抗菌评价分析了三位不同供体样本的生物膜形成与细菌活性(图3A-D)。通过SYTO 9/PI 荧光显微镜观察(图3B-C),获得了细菌活性的定性信息:钛金属表面死菌形成致密聚集的分布模式(图3C),而镁金属表面呈现活/死菌混杂的弥散簇状异质性分布(图5B)。这种空间分布特征与共聚焦三维重建结果(图3C)相印证,显示镁表面生物膜生物量低于钛表面。
扫描电镜分析(图3D)揭示了钛表面生物膜结构的供体差异性:供体1、2形成以链球菌为主的松散多层结构,供体3则呈现由球菌与球状菌构成的致密异质生物膜。值得注意的是,镁表面虽允许细菌粘附,但呈现独特的定殖模式:其微生物群落表现为球状菌、短杆菌及双球菌的簇状排列,且三位供体样本的生物膜厚度与细菌密度均一致低于钛表面。定量微生物学检测进一步验证了上述发现:基于CFU计数的定量分析(图3F-G)显示镁表面可培养菌落数显著低于钛表面(p < 0.05)。这些结果共同表明:镁表面虽允许细菌粘附,但能通过破坏生物膜结构与代谢过程,有效抑制生物膜成熟与细菌增殖。
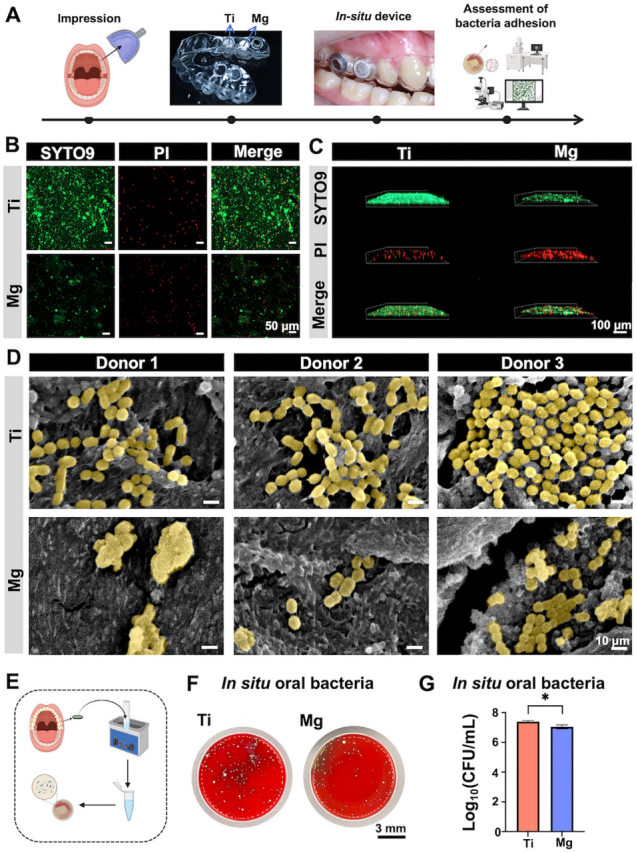
图3 原位模型中镁的抗菌性能评价
线性判别分析效应量(LEfSe)及KEGG通路富集分析揭示了不同供体对镁表面的特异性微生物特征及代谢响应(图4A-C)。LEfSe分析鉴定出在门水平上区分各供体镁组与钛对照组的分类学标志物(LDA评分>3)(图4A)。供体1在镁表面呈现链球菌属、孪生球菌属及聚生杆菌属的显著富集;供体2则表现为顶孢菌属、片球菌属和放线杆菌属的选择性增殖。值得注意的是,供体3的镁相关微生物群以棒状杆菌属、柠檬酸杆菌属及纤毛菌属为特征,表明存在供体特异的微生物筛选机制。
KEGG 通路富集分析显示的功能重编程模式与观察到的分类学变化相一致(图4B)。对比镁与钛金属表面,钛表面在三位供体中均显示出核心微生物维持通路上调,包括翻译(p=0.024)、复制/修复(p=0.013)及氨基酸代谢(p=0.011)。相反,镁表面引起广泛的代谢抑制,尤其在能量代谢(p=0.007)、信号转导(p=0.013)和核苷酸代谢(p=0.016)通路。三级通路分析进一步细化该趋势:钛表面显示核糖体生物合成(p=0.026)、氨酰-tRNA生物合成(p=0.016)和ABC转运蛋白活性(p=0.017)增强,而镁表面则表现出群体感应系统(p=0.017)、碳代谢(p=0.008)和嘧啶生物合成(p=0.017)的降低。
通过通路丰度的层次聚类分析,识别出供体特异性代谢响应(图4C)。供体1的微生物群表现出显著的代谢可塑性:钛表面强烈激活翻译、核苷酸代谢和氨基酸生物合成通路,而镁表面将这些通路抑制至接近基线水平。供体2呈现中等程度功能偏移,钛表面诱导聚糖生物合成和脂质代谢激活,但翻译机制变化较不显著。供体3的微生物群固有代谢活性较低,钛表面通路调控微弱,且能量生成通路即使在钛对照组中已处于基础抑制状态。
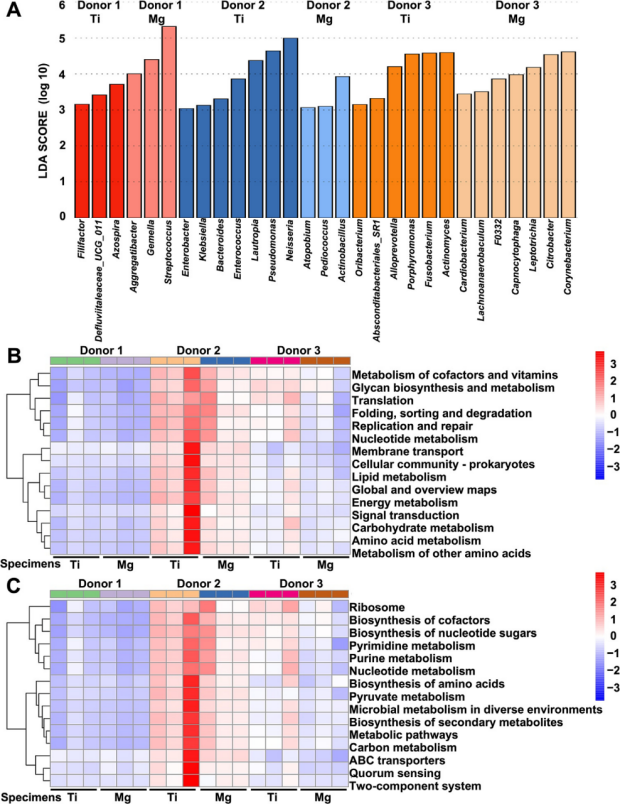
图4 镁金属表面菌群的线性判别分析效应量(LEfSe)以及KEGG通路富集分析
如图5示意图显示,口腔原位镁降解机制与其在体外微生物腐蚀存在本质差异,主要体现在三方面:首先,富含黏蛋白和釉质蛋白的唾液获得性薄膜可调控金属-组织界面电化学活性,其形成的吸附有机层作为屏障能降低离子交换速率,抑制局部腐蚀。其次,口腔动态的唾液流动通过稀释酸性产物并持续补充碳酸氢盐缓冲液,避免局部pH极端变化。第三,细菌相互作用模式显著不同:体外生物膜通过形成酸性微环境加剧腐蚀,而体内唾液剪切力抑制致病性生物膜成熟。更重要的是,体内形成了由氧化镁复合物、唾液获得性薄膜及黏附菌群构成的稳态腐蚀层。这种在静态体外系统中未观察到的自我调节降解模式,揭示了腐蚀产物参与表面钝化的保护性反馈机制。
在口内环境中镁主要呈现抑菌而非杀菌效应,这与降解介导的环境变化相一致。镁在体外抗菌作用涉及碱性环境导致的生理功能破坏及镁离子协同效应。然而在口腔环境中,唾液的缓冲能力会中和pH并减轻镁离子的作用,从而削弱上述效应。唾液缓冲系统能有效对抗碱性驱动机制,可能限制pH上升并降低对细菌细胞的渗透威胁。
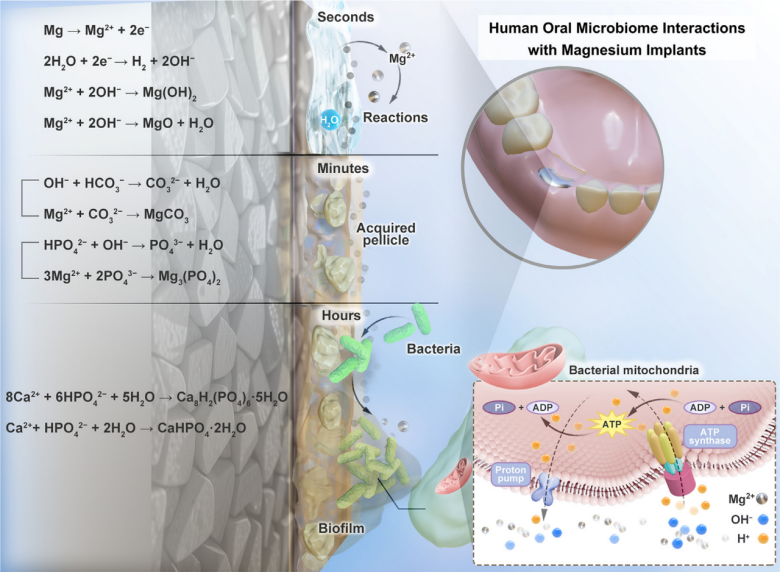
图5 镁与口腔生物膜之间双向互作关系的示意图
03、结论与展望
本研究揭示了纯镁与口腔微生物组之间的相互作用机制,阐明了其在口腔环境中调控材料腐蚀行为与生物学性能的基本规律。原位分析结果表明,镁与细菌的相互作用会诱导形成空间异质的腐蚀模式,这一过程通过生物矿化层的形成和有机基质的整合共同介导,并受到唾液流动状态及生物膜介导的缓冲作用的动态调控,最终实现抑制局部点蚀并促进材料均匀降解。
值得注意的是,尽管镁在体外表现出明显的抑菌特性,但在体内环境中,由于唾液蛋白与成熟生物膜胞外聚合物的离子螯合作用,其抗菌效果显著减弱。这导致微生物定殖呈现出显著的个体差异,该差异受到唾液流速等宿主特异性因素,以及早期生物膜群落中链球菌属相对优势度的共同影响。综上所述,本研究为镁基屏障膜的设计提供了重要依据。
04、文章信息
该文章发表在《Journal of Magnesium and Alloys》2025年:[1] Lian Huang, Wentai Zhang, Jiahao Chen, Franziska Schmidt, Yanyun Liu, Kai Chen, Janak Lal Pathak*, Zhentao Yu*, Ping Li*. Human oral microbiome interactions with magnesium implants. [J]. Journal of Magnesium and Alloys, 2025.
05、下载链接

扫描二维码下载文章!
06、中文摘要
镁基屏障膜作为引导骨再生的生物材料具有重要潜力,其临床应用前景广阔。然而,目前关于镁基植入体与人体口腔微生物组之间的相互作用机制仍不明确。本研究采用个性化口腔装置,对纯镁与人体口腔微生物组的双向相互作用进行了原位探究。结果表明:镁与细菌的相互作用可诱导形成空间异质的腐蚀层,该腐蚀层以生物矿化沉积和有机基质整合为特征;动态唾液流动与生物膜介导的扩散屏障共同作用,促进了均匀的电化学降解过程,并有效抑制了局部点蚀的发生。
尽管纯镁在体外表现出抗菌效应,但在体内环境中,因唾液对镁基表面的螯合作用及生物膜的成熟,其抑菌效果受到削弱,导致生物材料表面微生物定植呈现明显的个体差异。此外,链球菌属作为优势定植菌群,其定植模式受到获得性膜和唾液流速的影响。本研究阐明了人体口腔微生物组在调控镁腐蚀路径中的关键作用,为镁基屏障膜的设计提供了重要依据。
07、英文摘要
Magnesium (Mg)-based barrier membranes demonstrate significant potential as biomaterials for guided bone regeneration, thereby potentially broadening the scope of clinical applications. However, the interaction between Mg-based implants and the human oral microbiome remains poorly understood. This in situ human study investigated the bidirectional interactions between pure Mg and the human oral microbiome using a personalized oral device. The results demonstrated that Mg-bacteria interactions induce spatially heterogeneous corrosion layers characterized by biomineralized precipitates and organic-matrix integration. Dynamic salivary flow and biofilm-mediated diffusion barrier synergistically promoted uniform electrochemical degradation and suppressed localized pitting corrosion.
Although pure Mg exhibited antimicrobial effects under in vitro conditions, its in vivo bacteriostatic effect was attenuated by salivary sequestration of Mg-based surface and biofilm maturation. This led to inter-individual variability in microbial colonization of the biomaterial. Also, Streptococcus spp. were the dominant colonizers, and this pattern was influenced by acquired pellicle and salivary flow. These findings elucidate the critical role of the human oral microbiome in modulating Mg corrosion pathways, providing insights for the rational design of Mg-based implants for dental applications.
08、作者简介
第一作者/通讯作者简介
张文泰(共同第一作者),南方医科大学第十附属医院副研究员,作为项目负责人承担国家自然科学基金等科研项目5项。以第一/通讯作者在Advanced Functional Materials、Advanced Science等知名学术期刊上发表论文16篇,担任国际期刊Smart Materials in Medicine管理编辑。
黄链(共同第一作者),广州医科大学在读硕士研究生,主要从事镁基可降解金属的抗菌性能及耐腐蚀性能研究。
Janak Lal Pathak(通讯作者),广州医科大学副教授,博士生导师,主持国家自然科学基金等科研项目3项,发表SCI论文102 篇,其中通讯和第一作者(含共同)共63篇;累计影响因子 450分。担任Signal Transduction and Targeted Therapy、Bioactive Materials、ACS applied materials and Interfaces 等多本SCI 杂志的期刊审稿人。
于振涛(通讯作者),博士,暨南大学教授,博士生导师。国际生物材料科学与工程学会联合会(IUSBSE)生物材料科学与工程会士、中国生物材料学会首届会士,中国生物材料学会常务理事,中国生物材料口腔颅颌面材料分委会主委,中国腐蚀与防护学会常务理事等。主持国家重点研发计划等科研项目。获省部级一、二等奖13项,申/获国家发明(实用新型)专利100余项,主/参编专著7部。
李平(通讯作者),广州医科大学南山学者特聘教授、博士生导师。主要从事口腔修复学的临床、教学、科研工作。近5年,主持国家自然科学基金等科研项目6项,以第一/通讯作者身份(含共同)在Bioactive Materials、Biomaterials等高水平期刊发表SCI论文46篇。兼职中国生物材料学会口腔颅颌面材料分会委员等。










